(图片开端:DeepMind)火星电竞
刚刚,顶级科学期刊英国《Nature》(当然)杂志发表了一份重磅、冲突性琢磨论文。
北京时辰5月8日23点,DeepMind和其英国子公司Isomorphic Labs辘集团队在《当然》杂志上发表一份共46页的要紧遵循,辘集发布全新AI卵白质结构预测模子AlphaFold 3,可准确预测生物分子互相作用的结构。
具体来说,新的AlphaFold 3领有更强的生成式AI模子本事,效果全面莳植。对于卵白质与其他分子的互相作用,与现存预测方法比较,AlphaFold 3阅兵了至少50%;对于一些要紧的互相作用鸿沟,AlphaFold 3预测精(准确)度提高一倍(100%),可准确预测卵白质、DNA、RNA、配体等的结构以及它们如何互相作用,有望匡助东说念主们调节、免疫性疾病等。
稍早前举行的相通会上,本论文共同监督作家、谷歌DeepMind辘集首创东说念主、CEO戴姑娘•哈萨比斯(Demis Hassabis)对钛媒体App等示意,对于团队来说,AlphaFold 3的发布是一个要紧的“里程碑”,同期亦然用 AI 技能“剖析和建模生物学”说念路上迈出的要紧一步。
“比较此前琢磨,AlphaFold 3不仅八成模拟卵白质与其他分子的互相作用,而且还能准确预测包括DNA、RNA、配体等生物分子结构以及它们如何互相作用,从而能改动咱们对生物宇宙和药物发现的剖析,这荒谬要紧。这是咱们和Isomorphic共同正在鼓吹的事情。咱们荒谬自爱地在《当然》杂志新论文中晓示这些新冲突发现、新收尾和新方法。”Demis Hassabis示意。
对于AlphaFold 3的论文琢磨截图
六年超180万东说念主的卵白质数据库,AlphaFold 3模子预测精确再莳植一倍
AlphaFold是由谷歌DeepMind配置的一款卵白质结构预测法子,它汲取 AI 和深度学习技能仅凭据其基因序列就能预测卵白质的3D结构,仅需数日内可识别卵白质的局势,从而找到药物靶点,并有望鼓吹产生新的小分子药物。
而在此之前,研发一款药物,时时需要数年时辰、数亿好意思元的干与。
AlphaFold 1于2018年发布,其在CASP(卵白质结构预测的关键评估)竞赛中得手预测了43种卵白质中25种卵白质的最精确结构,名纪律一,并觉得得手预测了最贫困筹办的卵白质结构,激勉人人的温雅。
2020年,全新AlphaFold 2发布,并同步推出AlphaFold数据库,涵盖了东说念主类和20种常用款式生物的35万个卵白质结构,况且对98.5%的东说念主类卵白质结构进行了准确预测。同期,独特2.14亿个预测中约有35%被觉得是高度准确的,这意味着它们与实验笃定的结构一样好,另外45%被觉得对于很多应用来说充足准确。
2022年7月,AlphaFold 2全面升级,DeepMind公司与欧洲生物信息琢磨所(EMBL-EBI)的相助团队晓示,基于UniProt数据库序列,AlphaFold预测出约100万个物种的2亿多个卵白质结构,真实涵盖了扫数科学已知的卵白质。持续琢磨遵循发表在《当然》杂志上。
据Demis Hassabis透露的一份官方数据涌现,截止现在,AlphaFold数据库用户已达180万东说念主次,袒护超190个国度,已搜检的结构超600万次,论文和数据援用次数独特20000次。
谷歌DeepMind反复强调,通过减少冉冉而高亢的实验的需求,AlphaFold可能为琢磨界带来了数亿年的独特,并检朴了数万亿好意思元。数百万琢磨东说念主员人人范围内依然使用 AlphaFold 2 在疟疾疫苗、癌症调节和酶设想等鸿沟取得了发现。
参与相通会论说文作家包括Max Jaderberg、John Jumper、Julien Bergeron、Dhavanthi Hariharan和Josh Abramson,语音演讲是哈萨比斯(图片开端:钛媒体App剪辑拍摄)
6年后的今天,AlphaFold 3终于来了。
这次公布的AlphaFold 3,官方界说为一种由神经相聚架构构成、领有八成高精度预测包含卵白质数据库(PDB) 中真实扫数分子类型复合物的“生成式 AI 模子”。
钛媒体AGI基于DeepMind辘集发布这份对于AlphaFold 3的46页论文以及数十页的外部信息,梳理了AlphaFold 3模子锻练数据、推行经由、评测收尾以及交易化与生态四个层面,谈及新模子的要紧亮点:
1、模子锻练数据上,AlphaFold 3模子凭据卵白质数据库中包含的宇宙分子结构数据进行锻练,八成处理其中包含的 99% 以上的已知生物分子复合物。
2、推行经由层面,AlphaFold 3基于具备三角详确力的自界说Transformer构建,允许科学家输入生物分子复合物的描画,能预测该生物分子复合物的3D结构,并使用扩散经由生成每个原子的单独3D坐标,输入到指定系统。输入后,AlphaFold 3使用扩散相聚处理其预测,访佛于 AI 图像生成器中的相聚。扩散经由从原子云初始,经过很多门径集聚成最终的、最准确的分子结构。
而这一模子的中枢是DeepMind阅兵的Evoformer模块。AlphaFold 3 对分子互相作用的预测独特了扫数现存系统的准确性。
据论文涌现,据琢磨发现和使用经由看,AlphaFold 3的结构预测款式有助于创建与筹办卵白有用勾通的设想;同期,AlphaFold 3 提高了卵白质-卵白质界面的结构准确性,为设想新的调节神志(举例抗体或其他调节性卵白质)提供了可能性;另外,通过不雅察靶标在其完好生物学布景下的结构以及与其他卵白质勾通伴侣、DNA、RNA 或配体辅因子的复合体,不错更深化地了解新靶标,团队深信这种新的药物靶点寻找神志,八成飘浮为临床上更有用的药物。
DeepMind举了AlphaFold 3三个应用案例。
比如,整合膜卵白层面,AlphaFold 3正确预测了 PORCN 与 LGK974 和 WNT3A 肽的复合物,为该临床阶段分子 (PDB ID 7URD) 的支配功能提供了结构旨趣;变构位点鸿沟,PI5P4Kγ 是一种脂质激酶,与癌症和免疫性疾病持续,而AlphaFold 3正确预测新式支配剂 (PDB ID 7QIE) 的新式变构勾通款式;具有特有折叠的卵白质鸿沟,AlphaFold 3能正确预测与底物勾通的卵白质复合物的新折叠款式。
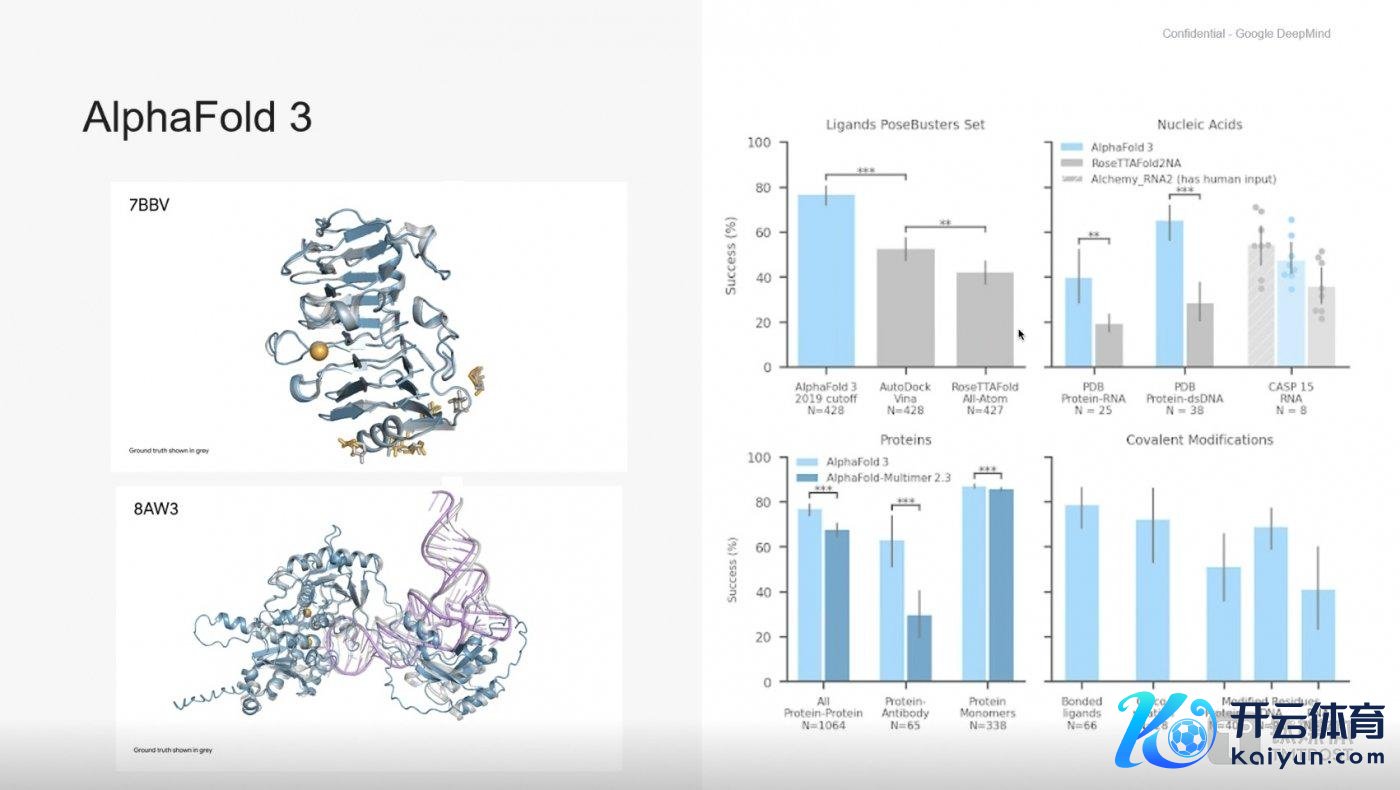
3、评测收尾。
据PoseBusters 基准集涌现,对于卵白质与小分子的互相作用,即使不使用任何结构输入,AlphaFold 3在76%的情况下得手了,而下一个最佳的器具惟有52%,大大优于Vina38、39等经典对接器具,况且大大优于 RoseTTAFold All-Atom 等扫数其他信得过的盲对接器具;同期,对于卵白质与DNA勾通的准确性,AlphaFold 3有65%的得手率,而现在的技能水平惟有28%。以至AlphaFold 3还阅兵了卵白质互相作用本事,当卵白质与抗体复杂勾通时,AlphaFold 3的准确得手率达62%,而其他系统惟有30%,比AlphaFold 2有约两倍的性能莳植。
此外,对于卵白质与其他分子的要紧互相作用鸿沟,AlphaFold 3预测准确度提高一倍(100%)。
4、交易化和生态。
AlphaFold 3不错模拟这些分子(卵白质)物资,这些分子限度着细胞的健康功能,要是受到梗阻,就会导致疾病,因此,AlphaFold 3不错应用于从生物学、可再生材料、食粮作物、剖析癌症、配置调节、金融等多个场景鸿沟。
Demis Hassabis坦言,DeepMind更多是作念基础琢磨,以便将AlphaFold提供给扫数学术机构、非交易用途等;而延误发现子公司Isomorphic Labs更多是作念交易化,与化学方面的药物发现存关,以及与大型药企相助配置世纪的药物发现名堂。
“改日,咱们将通过Isomorphic Labs和里面琢磨计算,并与咱们在Isomorphic Labs上的制药相助伙伴相助,进一步提高这些本事。”Demis Hassabis示意。
构建免费学术生态的同期,AlphaFold将经管AI药物发现的局限性
动作这次发布的一部分,DeepMind还推出AlphaFold 3免费 AI 器具AFServer,可供学术界免费使用,以构建AlphaFold生态。
DeepMind高档琢磨科学家John Jumper示意,剖析生物结构以及它们如何互相作用是一个荒谬贫困的问题。此前实验室需要挥霍数十万好意思元、更多科学家也很难通过实验模拟经管,但 AI 八成经管此类问题,这是令东说念主难以置信的独特,从而将“开启”很多新的科学发现。
Demis Hassabis强调,AlphaFold 3模子和数据库技能依然初始有一些应用场景,对于药物和化合物发现存雄伟的推动作用。相对于传统经由,AlphaFold至少快2、3倍,且系统充足准确。
然则现在,AlphaFold 3模子在立体化学、幻觉、能源学和某些筹办的准确性等方面仍存在一定局限性。
好意思国科学院外籍院士、好意思国艺术与科学院外籍院士、中国科学院院士,中国医学科学院学部委员、深圳医学科学院首创院长、深圳湾实验室主任、清华大学讲席教授颜宁曾示意,AlphaFold无法预测新的分子机构,预测出的结构其实仅仅达到其2017年的水平,艰辛专科锻练新的数据库(database),无法像东说念主一样兑现不同构念念和新使命机理,从而不行取得新的药物靶点。
颜宁强调,尽管看好 AI 技能的改日,但 AI 自己还口舌常有局限性的,需要有更大的数据库、更强的算力、更新的算法,才八成让 AI 形成结构生物学的要紧器具。
“对于小分子药物的互相作用,现在AlphaFold2的预测琢磨窝囊为力,短期内不看好AI取代实验,结构生物学的改日也不会是AI。”颜宁称。
DeepMind团队则在论文中指出,分子生物学的中枢挑战是剖析并最终调换生物系统复杂的原子互相作用。而AlphaFold 3模子朝这个标的迈出了一大步,评释不错在长入的框架中准确预测各式生物分子系统的结构。
“尽管在扫数交互类型中兑现高度准确的预测仍然存在要紧挑战,但团队评释,不错构建一个深度学习系统,对扫数这些交互涌现出强劲的袒护范围和泛化本事;同期还评释,艰辛跨实体进化信息并不是预测这些互相作用取得阐发的要紧支配;此外,AlphaFold孳生方法八成对分子互相作用类别的化学和物理进行建模,而无需对 MSA 的依赖,而且卵白质-配体结构预测的雄伟阅兵标明,不错在通用深度学习框架内处理化学空间的平淡各类性,而无需东说念主工分散卵白质结构预测和配体对接。”DeepMind团队称,设赠给确的深度学习框架不错大幅减少获取生物学数据所需的数据量。
预测改日,DeepMind琢磨东说念主员在交流中示意,团队将赓续埋头琢磨,从第一性旨趣开赴,用 AI 经管化学、生物学中前沿技能问题,从而有助于改动东说念主类设想下一代生物疗法神志,让科学家更多了解细胞系统的复杂性、结构、互相作用等,推动药物作用和研发等。
“固然这是 AI 驱动生物学琢磨的要紧时刻,但 AI 加快生物学的后劲是无尽的。AlphaFold AI 模子的进一步发展,将加深东说念主类对生物学和生命构建模块的剖析,以兑现咱们最终筹办——诓骗 AI 重构通盘药物发现经由。”论文琢磨团队示意。
(本文首发于钛媒体App,作家|林志佳,剪辑|胡润峰)